Ŝablono:Tabela informkesto
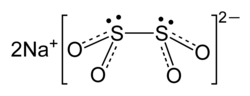
Natria dutionito, dutionito de natrio aŭ Na2S2O4 estas neorganika komponaĵo, blanka kristalo kun malforta sulfurodoro, rezultanta el natria hidroksido kaj dutionita acido. Kvankam ĝi plejparte estas stabila, ĝi malkomponiĝas en varma akvo kaj acidaj solvaĵoj. Kelkfoje ĉi-varmo sufiĉas por bruligi la ĉirkaŭantajn oksidivajn materialojn.
Ĝi estas akvosolvebla, kaj sub longedaŭra ekspozicio al fajro aŭ apudeco al varmaj enhavaĵoj, ĉi-materialo povas subite rompiĝi. Ĝi same uzatas en tinkturoj kaj blankigo de ligna pulpo.
Sintezoj
Sintezo 1
|
|
Sintezo 2
Sintezo 3
|
|
Sintezo 4
|
|
Sintezo 5
|
|
Sintezo 6
Sintezo 7
|
|
Reakcioj
Reakcio 1
- Ĝi malkomponiĝas kiam hejtata:
|
|
Reakcio 2
- La kristala salo estiĝas per hejtado de etanola solvaĵo:
|
|
Reakcio 3
- Per hejtata akvo ĝi suferas disproporcion:
|
|
Reakcio 4
- Ĝi malkomponiĝas en la ĉeesto de acido, malvarme:
|
|
Reakcio 5
|
|
Reakcio 6
- Ĝi spontanee oksidiĝas per la atmosfera oksigeno:
Reakcio 7
|
|
Reakcio 8
- Ĝi restarigas la metalojn malpli aktivajn:
|
|
Literaturo
Ŝablono:Neorganikaj saloj de natrio
Ŝablono:Organikaj saloj de natrio
Ŝablono:Portalo
Ŝablono:Projektoj
Ŝablono:Ĝermo