Kalia fenoksido
Ŝablono:Vidu ankaŭ Ŝablono:Tabela informkesto
| Kalia fenoksido | |
 | |
| Plata kemia strukturo de la Kalia fenoksido | |
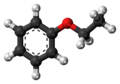
| Tridimensia kemia strukturo de la Kalia fenoksido | |
| Alternativa(j) nomo(j) | |
| |
| Kemia formulo | |
| CAS-numero-kodo | 100-67-4 |
| ChemSpider kodo | 8305495 |
| PubChem-kodo | 23670670 |
| Fizikaj proprecoj | |
| Molmaso | 132,203 g·mol−1 |
| Bolpunkto | Ŝablono:GdC[1] |
| Ekflama temperaturo | Ŝablono:GdC |
| Sekurecaj Indikoj | |
| Riskoj | R22 R34 |
| Sekureco | S20 S26 S36/37/39 S45 S60 |
| Pridanĝeraj indikoj | |
| Danĝero Ŝablono:Danĝerosimboloj | |
| GHS Damaĝo Piktogramo | |
| GHS Signalvorto | Damaĝa substanco |
| GHS Deklaroj pri damaĝoj | Ŝablono:H-Frazoj |
| GHS Deklaroj pri antaŭgardoj | Ŝablono:P-Frazoj |
(Ŝablono:GdC kaj 100 kPa) | |
Kalia fenoksido aŭ C6H5KO estas organika kombinaĵo, blanka solidaĵo kun konjuga bazo de fenolo. Ĝi uzatas kiel antaŭanto de aliaj organikaj komponaĵoj, same kiel arilaj eteroj. Plej ordinare, solvaĵoj de kalia fenoksido estiĝas per traktado de fenolo kaj kalia hidroksido. Anhidraj derivaĵoj estas prepareblaj ekde fenolo kaj kalio.
Sintezoj
Sintezo 1
|
2 kalio + 2 fenolo2 kalia fenoksido+ hidrogeno |
Sintezo 2
- Preparado de kalia fenoksido per traktado de benzenosulfonata acido kaj kalia hidroksido:
|
|
Sintezo 3
- Per traktado de la natria metoksido kun fenolo:
Sintezoj kaj reakcioj
Reakcio 1
- Reakcio inter fenolo kaj kalia hidroksido:
Reakcio 2
- Reakcio inter fenolo kaj kalia bikarbonato:
Reakcio 3
- Preparado de fenolo ekde kalia fenoksido:
Reakcio 4
- Kalia salikato estiĝas pere de reakcio inter kalia fenoksido kaj karbona duoksido:
Reakcio 5
- Kalia fenoksido reakcias kun etila bromido estigante fenetolon aŭ fenil-etil-eteron:
Reakcio 6
- Kalia fenoksido reakcias kun metila bromido estigante anizolon aŭ fenil-metil-eteron:
Reakcio 7
- La graveco de ĉi-komponaĵo kuŝas en la produktado de salikata acido. Unue la fenolato de kalio reakcias kun karbona duoksido sub varmo kaj forta premo por formi kalian salikaton. Due, en acida medio, salikato de kalio estas neŭtraligita en ĉeesto de acidoj por formi la salikatan acidon:[2]
Literaturo
- Alfa Chemistry
- Thermal Analysis
- Journal of Applied Chemistry of the USSR
- Chemical Structure and Reactivity: An Integrated Approach
- Journal of the Indian Chemical Society
Referencoj
Ŝablono:Neorganikaj saloj de kalio Ŝablono:Organikaj saloj de kalio Ŝablono:Projektoj Ŝablono:Ĝermo