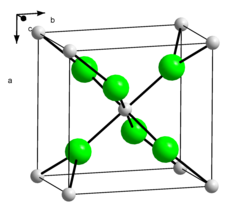
Kalcia klorido
Kalcia klorido estas senkolora aŭ blanka kristala higroskopa solido, neorganika kombinaĵo alte solvebla en akvo. Ĉi-kombinaĵo trovatas en multaj hidratigitaj formulaĵoj kaj uzatas kiel elsekigaĵo en laboratorio kaj industrio kaj kiel medikamento en la traktado de malsanoj kie okazas manko de kalcio en la organismo. Pro tio ke ĝi enhavas la kalcian jonon, ĝi uzatas kiel precipitanto en la traktado de eluzita akvo.
Sintezoj
Sintezo 1
Klorido de kalcio estiĝas per interagado de la kalcia karbonato kaj klorida acido donante kiel subproduktoj karbonan duoksidon kaj akvon:
|
|
Sintezo 2
- Kalcia klorido ankaŭ prepareblas per agado de la amonia klorido sur kalcia hidroksido:
|
|
Reakcio
Kalcia klorido reakcias kun kalia fosfato por doni kalcian fosfaton kaj KCl:
Literaturo
- LiveStrong
- Drugbank
- Merck Millipore
- Peters Chemical Company
- Calcium Chloride Recovery in Soda Ash Production by Solvay's Process, Temesgen Atnafu, Seid Yimer
- Molten Salts and Ionic Liquids 16, Edição 49, D. Fox
Vidu ankaŭ
- Kalcia karbonato
- Kalcia cianamido
- Natria karbonato
- Kalcia karbido
- Acetileno
- Natria klorido
- Procezo Solvay